Сильные электролиты при растворении в воде практически полностью диссоциируют на ионы независимо от их концентрации в растворе.
Поэтому в уравнениях диссоциации сильных электролитов ставят знак равенства (=).
К сильным электролитам относятся:
Растворимые соли;
Многие неорганические кислоты: HNO3, H2SO4, HCl, HBr, HI;
Основания, образованные щелочными металлами (LiOH, NaOH, KOH и т.д.) и щелочно-земельными металлами (Ca(OH)2, Sr(OH)2, Ba(OH)2).
Слабые электролиты в водных растворах лишь частично (обратимо) диссоциируют на ионы.
Поэтому в уравнениях диссоциации слабых электролитов ставят знак обратимости (⇄).
К слабым электролитам относятся:
Почти все органические кислоты и вода;
Некоторые неорганические кислоты: H2S, H3PO4, H2CO3, HNO2, H2SiO3 и др.;
Нерастворимые гидроксиды металлов: Mg(OH)2, Fe(OH)2, Zn(OH)2 и др.
Ионные уравнения реакций
Ионные уравнения реакций
Химические реакции в растворах электролитов (кислот, оснований и солей) протекают при участии ионов. Конечный раствор может остаться прозрачным (продукты хорошо растворимы в воде) , но один из продуктом окажется слабым электролитом; в других случаях будет наблюдаться выпадение осадка или выделение газа.
Для реакций в растворах при участии ионов составляют не только молекулярное уравнение, но также полное ионное и краткое ионное.
В ионных уравнениях по предложению французского химика К. -Л. Бертолле (1801 г.) все сильные хорошо растворимые электролиты записывают в виде формул ионов, а осадки, газы и слабые электролиты - в виде молекулярных формул. Образование осадков отмечают знаком "стрелка вниз" (↓), образование газов - знаком "стрелка вверх" (). Пример записи уравнения реакции по правилу Бертолле:
а) молекулярное уравнение
Na2CO3 + H2SO4 = Na2SO4 + CO2 + H2O
б) полное ионное уравнение
2Na+ + CO32− + 2H+ + SO42− = 2Na+ + SO42− + CO2 + H2O
(CO2 - газ, H2O - слабый электролит)
в) краткое ионное уравнение
CO32− + 2H+ = CO2 + H2O
Обычно при записи ограничиваются кратким ионным уравнением, причем твердые вещества-реагенты обозначают индексом (т) , газобразные реагенты - индексом (г) . Примеры:
1) Cu(OH)2(т) + 2HNO3 = Cu(NO3)2 + 2H2O
Cu(OH)2(т) + 2H+ = Cu2+ + 2H2O
Cu(OH)2 практически нерастворим в воде
2) BaS + H2SO4 = BaSO4↓ + H2S
Ba2+ + S2− + 2H+ + SO42− = BaSO4↓ + H2S
(полное и краткое ионное уравнения совпадают)
3) CaCO3(т) + CO2(г) + H2O = Ca(HCO3)2
CaCO3(т) + CO2(г) + H2O = Ca2+ + 2HCO3−
(большинство кислых солей хорошо растворимы в воде) .
Если в реакции не участвуют сильные электролиты, ионный вид уравнения отсутствует:
Mg(OH)2(т) + 2HF(р) = MgF2↓ + 2H2O
БИЛЕТ №23
Гидролиз солей
Гидролиз солей – это взаимодействие ионов соли с водой с образованием малодиссоциирующих частиц.
Гидролиз, дословно, - это разложение водой. Давая такое определение реакции гидролиза солей, мы подчеркиваем, что соли в растворе находятся в виде ионов, и что движущей силой реакции является образование малодиссоциирующих частиц (общее правило для многих реакций в растворах).
Гидролиз происходит лишь в тех случаях, когда ионы, образующиеся в результате электролитической диссоциации соли - катион, анион, или оба вместе, - способны образовывать с ионами воды слабодиссоциирующие соединения, а это, в свою очередь, происходит тогда, когда катион - сильно поляризующий (катион слабого основания) , а анион - легко поляризуется (анион слабой кислоты). При этом изменяется рН среды. Если же катион образует сильное основание, а анион - сильную кислоту, то они гидролизу не подвергаются.
1.Гидролиз соли слабого основания и сильной кислоты проходит по катиону, при этом может образоваться слабое основание или основная соль и рН раствора уменьшится
2.Гидролиз соли слабой кислоты и сильного основания проходит по аниону, при этом может образоваться слабая кислота или кислая соль и рН раствора увеличится
3.Гидролиз соли слабого основания и слабой кислоты обычно проходит нацело с образованием слабой кислоты и слабого основания; рН раствора при этом незначительно отличается от 7 и определяется относительной силой кислоты и основания
4.Гидролиз соли сильного основания и сильной кислоты не протекает
Вопрос 24 Классификация оксидов
Оксидами называются сложные вещества, в состав молекул которых входят атомы кислорода в степни окисления – 2 и какого-нибудь другого элемента.
Оксиды могут быть получены при непосредственном взаимодействии кислорода с другим элементом, так и косвенным путём (например, при разложении солей, оснований, кислот). В обычных условиях оксиды бывают в твёрдом, жидком и газообразном состоянии, этот тип соединений весьма распространён в природе. Оксиды содержатся в Земной коре. Ржавчина, песок, вода, углекислый газ – это оксиды.
Солеобразующие оксиды Например,
CuO + 2HCl → CuCl 2 + H 2 O.
CuO + SO 3 → CuSO 4 .
Солеобразующие оксиды – это такие оксиды, которые в результате химических реакций образуют соли. Это оксиды металлов и неметаллов, которые при взаимодействии с водой образуют соответствующие кислоты, а при взаимодействии с основаниями – соответствующие кислые и нормальные соли. Например, оксид меди (CuO) является оксидом солеобразующим, потому что, например, при взаимодействии её с соляной кислотой (HCl) образуется соль:
CuO + 2HCl → CuCl 2 + H 2 O.
В результате химических реакций можно получать и другие соли:
CuO + SO 3 → CuSO 4 .
Несолеобразующими оксидами называются такие оксиды, которые не образуют солей. Примером могут служить СО, N 2 O, NO.
ЭЛЕКТРОЛИТЫ – вещества, растворы или расплавы которых проводят электрический ток.
НЕЭЛЕКТРОЛИТЫ – вещества, растворы или расплавы которых не проводят электрический ток.
Диссоциация – распад соединений на ионы.
Степень диссоциации – отношение числа продиссоциированных на ионы молекул к общему числу молекул в растворе.
СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ при растворении в воде практически полностью диссоциируют на ионы.
При написании уравнений диссоциации сильных электролитов ставят знак равенства.
К сильным электролитам относятся:
· Растворимые соли (смотри таблицу растворимости );
· Многие неорганические кислоты: HNO 3 , H 2 SO 4 ,HClO 3 , HClO 4 , HMnO 4 , HCl, HBr, HI (смотри кислоты-сильные электролиты в таблице растворимости );
· Основания щелочных (LiOH, NaOH,KOH) и щелочноземельных (Ca(OH) 2 , Sr(OH) 2 , Ba(OH) 2) металлов (смотри основания-сильные электролиты в таблице растворимости ).
СЛАБЫЕ ЭЛЕКТРОЛИТЫ в водных растворах лишь частично (обратимо) диссоциируют на ионы.
При написании уравнений диссоциации слабых электролитов ставят знак обратимости.
К слабым электролитам относятся:
· Почти все органические кислоты и вода (Н 2 О);
· Некоторые неорганические кислоты: H 2 S, H 3 PO 4 ,HClO 4 , H 2 CO 3 , HNO 2 , H 2 SiO 3 (смотри кислоты-слабые электролиты в таблице растворимости );
· Нерастворимые гидроксиды металлов (Mg(OH) 2 ,Fe(OH) 2 , Zn(OH) 2) (смотри основания- c лабые электролиты в таблице растворимости ).
На степень электролитической диссоциации влияет ряд факторов:
природа растворителя и электролита : сильными электролитами являются вещества с ионными и ковалентными сильно-полярными связями; хорошей ионизирующей способностью, т.е. способностью вызывать диссоциацию веществ, обладают растворители с большой диэлектрической проницаемостью, молекулы которых полярны (например, вода);
температура : поскольку диссоциация - процесс эндотермический, повышение температуры повышает значение α;
концентрация : при разбавлении раствора степень диссоциации возрастает, а с увеличением концентрации - уменьшается;
стадия процесса диссоциации : каждая последующая стадия менее эффективна, чем предыдущая, примерно в 1000–10 000 раз; например, для фосфорной кислоты α 1 > α 2 > α 3:
H3PО4⇄Н++H2PО−4 (первая стадия, α 1),
H2PО−4⇄Н++HPО2−4 (вторая стадия, α 2),
НPО2−4⇄Н++PО3−4 (третья стадия, α 3).
По этой причине в растворе данной кислоты концентрация ионов водорода наибольшая, а фосфат-ионов РО3−4 - наименьшая.
1. Растворимость и степень диссоциации вещества между собой не связаны. Например, слабым электролитом является хорошо (неограниченно) растворимая в воде уксусная кислота.
2. В растворе слабого электролита меньше других содержится тех ионов, которые образуются на последней стадии электролитической диссоциации
На степень электролитической диссоциации влияет также добавление других электролитов : например, степень диссоциации муравьиной кислоты
HCOOH ⇄ HCOO − + H +
уменьшается, если в раствор внести немного формиата натрия. Эта соль диссоциирует с образованием формиат-ионов HCOO − :
HCOONa → HCOO − + Na +
В результате в растворе концентрация ионов НСОО– повышается, а согласно принципу Ле Шателье, повышение концентрации формиат-ионов смещает равновесие процесса диссоциации муравьиной кислоты влево, т.е. степень диссоциации уменьшается.
Закон разбавления Оствальда - соотношение, выражающее зависимость эквивалентной электропроводностиразбавленного раствора бинарного слабого электролита от концентрации раствора:
Здесь - константа диссоциации электролита, - концентрация, и - значения эквивалентной электропроводности при концентрации и при бесконечном разбавлении соответственно. Соотношение является следствием закона действующих масс и равенства
где - степень диссоциации.
Закон разбавления Оствальда выведен В.Оствальдом в 1888 году и им же подтвержден опытным путём. Экспериментальное установление правильности закона разбавления Оствальда имело большое значение для обоснования теории электролитической диссоциации.
Электролитическая диссоциация воды. Водородный показатель рН Вода представляет собой слабый амфотерный электролит: Н2О Н+ + ОН- или, более точно: 2Н2О= Н3О+ + ОН- Константа диссоциации воды при 25оС равна: Такое значение константы соответствует диссоциации одной из ста миллионов молекул воды, поэтому концентрацию воды можно считать постоянной и равной 55,55 моль/л (плотность воды 1000 г/л, масса 1 л 1000 г, количество вещества воды 1000г:18г/моль=55,55 моль, С=55,55 моль: 1 л =55,55 моль/л). Тогда Эта величина постоянная при данной температуре (25оС), она называется ионным произведением воды KW: Диссоциация воды – процесс эндотермический, поэтому с повышением температуры в соответствии с принципом Ле-Шателье диссоциация усиливается, ионное произведение возрастает и достигает при 100оС значения 10-13. В чистой воде при 25оС концентрации ионов водорода и гидроксила равны между собой: = = 10-7 моль/л Растворы, в которых концентрации ионов водорода и гидроксила равны между собой, называются нейтральными. Если к чистой воде прибавить кислоту, концентрация ионов водорда повысится и станет больше, чем 10-7 моль/л, среда станет кислой, при этом концентрация ионов гидроксила мгновенно изменится так, чтобы ионное произведение воды сохранило свое значение 10-14. Тоже самое будет происходить и при добавлении к чистой воде щелочи. Концентрации ионов водорода и гидроксила связаны между собой через ионное произведение, поэтому, зная концентрацию одного из ионов, легко вычислить концентрацию другого. Например, если = 10-3 моль/л, то = KW/ = 10-14/10-3 = 10-11 моль/л, или, если = 10-2 моль/л, то = KW/ = 10-14/10-2 = 10-12 моль/л. Таким образом, концентрация ионов водорода или гидроксила может служить количественной характеристикой кислотности или щелочности среды. На практике пользуются не концентрациями ионов водорода или гидроксила, а водородным рН или гидроксильным рОН показателями. Водородный показатель рН равен отрицательному десятичному логарифму концентрации ионов водорода: рН = - lg Гидроксильный показатель рОН равен отрицательному десятичному логарифму концентрации ионов гидроксила: рОН = - lg Легко показать, прологарифмировав ионное произведение воды, что рН + рОН = 14 Если рН среды равен 7 - среда нейтральная, если меньше 7 - кислая, причем чем меньше рН, тем выше концентрация ионов водорода. pН больше 7 – среда щелочная, чем больше рН, тем выше концентрация ионов гидроксила.
, , 21 , , ,
, 25-26 , 27-28 ,
, 30, , , , , , , , /2003
§ 6.3. Сильные и слабые электролиты
Материал этого раздела частично вам знаком по ранее изученным школьным курсам химии и из предыдущего раздела. Кратко повторим, что вам известно, и познакомимся с новым материалом.
В предыдущем разделе мы обсуждали поведение в
водных растворах некоторых солей и органических
веществ, полностью распадающихся на ионы в
водном растворе.
Имеется ряд простых, но несомненных
доказательств того, что некоторые вещества в
водных растворах распадаются на частицы. Так,
водные растворы серной H 2 SO 4 , азотной HNO 3 ,
хлорной HClO 4 , хлороводородной (соляной) HCl,
уксусной CH 3 COOH и других кислот имеют кислый
вкус. В формулах кислот общей частицей является
атом водорода, и можно предположить, что он (в
виде иона) является причиной одинакового вкуса
всех этих столь различных веществ.
Образующиеся при диссоциации в водном растворе
ионы водорода придают раствору кислый вкус,
поэтому такие вещества и названы кислотами. В
природе только ионы водорода имеют кислый вкус.
Они создают в водном растворе так называемую
кислотную (кислую) среду.
Запомните, когда вы говорите «хлороводород», то имеете в виду газообразное и кристаллическое состояние этого вещества, но для водного раствора следует говорить «раствор хлороводорода», «хлороводородная кислота» или использовать общепринятое название «соляная кислота», хотя состав вещества в любом состоянии выражается одной и той же формулой – НСl.
Водные растворы гидроксидов лития (LiOH), натрия
(NаОН), калия (КОН), бария (Ва(ОН) 2), кальция
(Са(ОН) 2) и других металлов имеют одинаковый
неприятный горько-мыльный вкус и вызывают на
коже рук ощущение скольжения. По-видимому, за это
свойство ответственны гидроксид-ионы ОН – ,
входящие в состав таких соединений.
Хлороводородная HCl, бромоводородная HBr и
йодоводородная HI кислоты реагируют с цинком
одинаково, несмотря на свой различный состав, т.
к. в действительности с цинком реагирует не
кислота:
Zn + 2НСl = ZnСl 2 + Н2,
а ионы водорода:
Zn + 2H + = Zn 2+ + Н 2 ,
и образуются газообразный водород и ионы цинка.
Смешивание некоторых растворов солей, например
хлорида калия KCl и нитрата натрия NaNO 3 , не
сопровождается заметным тепловым эффектом, хотя
после выпаривания раствора образуется смесь
кристаллов четырех веществ: исходных – хлорида
калия и нитрата натрия – и новых – нитрата калия
КNO 3 и хлорида натрия NaCl. Можно предположить,
что в растворе две исходные соли полностью
распадаются на ионы, которые при его выпаривании
образуют четыре кристаллических вещества:
Сопоставляя эти сведения с
электропроводностью водных растворов кислот,
гидроксидов и солей и с рядом других положений,
С.А.Аррениус в 1887 г. выдвинул гипотезу
электролитической диссоциации, согласно которой
молекулы кислот, гидроксидов и солей при
растворении их в воде диссоциируют на ионы.
Изучение продуктов электролиза позволяет
приписать ионам положительные или отрицательные
заряды. Очевидно, если кислота, например азотная
НNO 3 , диссоциирует, предположим, на два иона
и при электролизе водного раствора на катоде
(отрицательно заряженный электрод) выделяется
водород, то, следовательно, в растворе имеются
положительно заряженные ионы водорода Н + .
Тогда уравнение диссоциации следует записать
так:
НNO 3 = Н + + .
Электролитическая диссоциация
–
полный или частичный распад соединения при его
растворении в воде на ионы в результате
взаимодействия с молекулой воды (или другого
растворителя).
Электролиты
– кислоты, основания или
соли, водные растворы которых проводят
электрический ток в результате диссоциации.
Вещества, не диссоциирующие в водном растворе на
ионы и растворы которых не проводят
электрический ток, называются неэлектролитами
.
Диссоциация электролитов количественно
характеризуется степенью диссоциации
– отношением числа распавшихся на ионы
«молекул» (формульных единиц) к общему числу
«молекул» растворенного вещества. Степень
диссоциации обозначается греческой буквой . Например, если из
каждых 100 «молекул» растворенного вещества 80
распадаются на ионы, то степень диссоциации
растворенного вещества равна: = 80/100 = 0,8, или 80%.
По способности к диссоциации (или, как говорят,
«по силе») электролиты разделяют на сильные
,
средние
и слабые
. По степени
диссоциации к сильным электролитам относят те из
них, для растворов которых > 30%, к слабым – < 3%, к средним – 3% 30%. Сила электролита –
величина, зависящая от концентрации вещества,
температуры, природы растворителя и др.
В случае водных растворов
к сильным электролитам
( > 30%) относят
перечисленные ниже группы соединений.
1
. Многие неорганические кислоты,
например хлороводородная НCl, азотная HNO 3 ,
серная H 2 SО 4 в разбавленных растворах.
Самая сильная неорганическая кислота – хлорная
НСlО 4 .
Сила некислородных кислот возрастает в ряду
однотипных соединений при переходе вниз по
подгруппе кислотообразующих элементов:
HCl – HBr – HI.
Фтороводородная (плавиковая) кислота HF растворяет стекло, но это вовсе не говорит о ее силе. Эта кислота из бескислородных галогенсодержащих относится к кислотам средней силы из-за высокой энергии связи Н–F, способности молекул HF к объединению (ассоциации) благодаря сильным водородным связям, взаимодействия ионов F – с молекулами НF (водородные связи) с образованием ионов и других более сложных частиц. В результате концентрация ионов водорода в водном растворе этой кислоты оказывается значительно пониженной, поэтому фтороводородную кислоту считают средней силы.
Фтороводород реагирует с диоксидом кремния, входящим в состав стекла, по уравнению:SiO 2 + 4HF = SiF 4 + 2H 2 O.
Фтороводородную кислоту нельзя хранить в стеклянных сосудах. Для этого используют сосуды из свинца, некоторых пластмасс и стекла, стенки которых покрыты изнутри толстым слоем парафина. Если для «травления» стекла использовать газообразный фтороводород, то поверхность стекла становится матовой, что используется для нанесения на стекло надписей и различных рисунков. «Травление» стекла водным раствором фтороводородной кислоты приводит к разъеданию поверхности стекла, которая остается прозрачной. В продаже обычно бывает 40%-й раствор плавиковой кислоты.
Сила однотипных кислородных кислот изменяется
в противоположном направлении, например йодная
кислота НIО 4 слабее хлорной кислоты НСlО 4 .
Если элемент образует несколько кислородных
кислот, то наибольшей силой обладает кислота, в
которой кислотообразующий элемент имеет самую
высокую валентность. Так, в ряду кислот НСlО
(хлорноватистая) – НСlО 2 (хлористая) – НСlО 3
(хлорноватая) – НСlО 4 (хлорная) последняя
наиболее сильная.
Один объем воды растворяет около двух объемов хлора. Хлор (примерно половина его) взаимодействует с водой:
Cl 2 + H 2 O = HCl + HСlO.
Хлороводородная кислота является сильной, в ее водном растворе практически нет молекул HCl. Правильнее уравнение реакции записать так:
Cl 2 + H 2 O = H + + Cl – + HClO – 25 кДж/моль.
Образующийся раствор называют хлорной водой.
Хлорноватистая кислота – быстродействующий окислитель, поэтому ее применяют для отбеливания тканей.
2 . Гидроксиды элементов главных подгрупп I и II групп периодической системы: LiОН, NaОН, КОН, Са(ОН) 2 и др. При переходе вниз по подгруппе по мере усиления металлических свойств элемента сила гидроксидов возрастает. Растворимые гидроксиды главной подгруппы I группы элементов относят к щелочам.
Щелочами называют растворимые в воде основания. К ним относят также гидроксиды элементов главной подгруппы II группы (щелочно-земельные металлы) и гидроксид аммония (водный раствор аммиака). Иногда щелочами считают те гидроксиды, которые в водном растворе создают высокую концентрацию гидроксид-ионов. В устаревшей литературе вы можете встретить в числе щелочей карбонаты калия К 2 СО 3 (поташ) и натрия Na 2 CO 3 (сода), гидрокарбонат натрия NaHCO 3 (питьевая сода), буру Na 2 B 4 O 7 , гидросульфиды натрия NaHS и калия KHS и др.
Гидроксид кальция Са(ОН) 2 как сильный электролит диссоциирует в одну ступень:
Са(ОН) 2 = Са 2+ + 2ОН – .
3 . Почти все соли. Соль, если это сильный электролит, диссоциирует в одну ступень, например хлорид железа:
FeCl 3 = Fe 3+ + 3Cl – .
В случае водных растворов к слабым электролитам ( < 3%) относят перечисленные ниже соединения.
1 . Вода H 2 O – важнейший электролит.
2
. Некоторые неорганические и почти
все органические кислоты: H 2 S
(сероводородная), H 2 SO 3 (сернистая), H 2 CO 3
(угольная), HCN (циановодородная), Н 3 РО 4
(фосфорная, ортофосфорная), H 2 SiO 3
(кремниевая), H 3 BO 3 (борная, ортоборная),
СН 3 СООН (уксусная) и др.
Заметим, что угольная кислота в формуле H 2 CO 3
не существует. При растворении углекислого газа
СО 2 в воде образуется его гидрат СО 2 Н 2 О,
который мы для удобства расчетов записываем
формулой H 2 CO 3 , и уравнение реакции
диссоциации выглядит так:
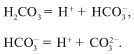
Диссоциация слабой угольной кислоты проходит в
две ступени. Образующийся гидрокарбонат-ион также ведет себя
как слабый электролит.
Точно так же ступенчато диссоциируют и другие
многоосновные кислоты: Н 3 РО 4
(фосфорная), H 2 SiO 3 (кремниевая), H 3 BO 3
(борная). В водном растворе диссоциация
практически проходит лишь по первой ступени. Как
осуществить диссоциацию по последней ступени?
3
. Гидроксиды многих элементов, например
Аl(OH) 3 , Cu(OH) 2 , Fe(OH) 2 , Fe(OH) 3 и др.
Все эти гидроксиды диссоциируют в водном
растворе ступенчато, например гидроксид железа
Fe(OH) 3:

В водном растворе диссоциация проходит
практически только по первой ступени. Как
сместить равновесие в сторону образования ионов
Fe 3+ ?
Осно"вные свойства гидроксидов одного и того же
элемента усиливаются с уменьшением валентности
элемента. Так, осно"вные свойства дигидроксида
железа Fe(OH) 2 выражены сильнее, чем у
тригидроксида Fe(OH) 3 . Это утверждение
равносильно тому, что кислотные свойства Fe(OH) 3
проявляются сильнее, чем у Fe(OH) 2 .
4
. Гидроксид аммония NH 4 OH.
При растворении газообразного аммиака NH 3 в
воде получается раствор, который очень слабо
проводит электрический ток и имеет
горько-мыльный вкус. Среда раствора осно"вная,
или щелочная. Объясняется такое поведение
аммиака следующим образом. При растворении
аммиака в воде образуется гидрат аммиака NH 3 Н 2 О,
которому условно мы приписываем формулу
несуществующего гидроксида аммония NH 4 OH,
считая, что это соединение диссоциирует с
образованием иона аммония и гидроксид-иона ОН – :
NH 4 OH = + ОН – .
5 . Некоторые соли: хлорид цинка ZnCl 2 , тиоцианат железа Fe(NСS) 3 , цианид ртути Hg(CN) 2 и др. Эти соли диссоциируют ступенчато.
К электролитам средней силы некоторые относят фосфорную кислоту Н 3 РО 4 . Мы будем считать фосфорную кислоту слабым электролитом и записывать три ступени ее диссоциации. Серная кислота в концентрированных растворах ведет себя как электролит средней силы, а в очень концентрированных растворах – как слабый электролит. Мы далее будем считать серную кислоту сильным электролитом и записывать уравнение ее диссоциации в одну ступень.
Электрический ток – направленное движение заряженных частиц – электронов или ионов.
Электролиты – это вещества, растворы или расплавы (в ЕГЭ чаще речь о растворах) которых проводят электрический ток, то есть содержат заряженные частицы. Свободных электронов в растворе не бывает, носителями заряда являются ионы. Электрический ток проводят расплавы веществ с ионной кристаллической решеткой.
К электролитам относятся:
- Кислоты
- Основания
Чем больше в растворе заряженных частиц, тем лучше он проводит электрический ток, т.е. чем больше молекул вещества диссоциирует, тем более сильным электролитом оно является.
Список сильных и слабых электролитов нужно знать наизусть!
Сильные электролиты (в растворах): 11
- Растворимые соли
FeCl 3 , CuSO 4 , K 2 CO 3 и т.д.
- Щелочи
8 растворимых гидроксидов: LiOH, NaOH, KOH, RbOH, CsOH, Ba(OH) 2 , Sr(OH) 2 , Ca(OH) 2 .
- Сильные кислоты
HI, HBr, HCl, H 2 SO 4(разб) , HNO 3 , HClO 4 , HClO 3 , HMnO 4 , H 2 CrO 4
Слабые электролиты:
- Слабые основания
нерастворимые гидроксиды, NH 3 ∙H 2 O, растворы аминов
- Слабые кислоты и кислоты средней силы
H 3 PO 4 , HF, H 2 SO 3 , H 2 CO 3 , H 2 S, H 2 SiO 3 , органические кислоты.
- Вода
H 2 O – очень слабый электролит, диссоциирует ничтожно мало. Чистая дистиллированная вода не проводит ток.
Неэлектролиты: большинство органических соединений, оксиды, вещества, в молекулах которых имеются только ковалентные неполярные или малополярные связи и т.д.
Сила электролита определяется степенью диссоциации. Рассмотрим соль А 2 В и кислоту Н 3 Х:
Диссоциация - всегда обратимый процесс.
Соли диссоциируют (обратимо распадаются на ионы) почти на 100%:
А 2 В ⇄ 2А + + В 2- . Так как все молекулы распались на ионы, из 1 моль АВ получилось 1 моль В 2- и 2 моль А + , то есть три моль ионов.
Многоосновные кислоты и основания диссоциируют ступенчато:
Н 3 Х ⇄ H + + H 2 X -
H 2 X - ⇄ HX 2- + H +
HX 2- ⇄X 3- + H +
При этом каждая следующая ступень диссоциации протекает хуже предыдущей, т.к. присутсвует конкурирующий процесс - обратная реакция. Порядок примерно такой: Из 1 моль молекул слабой кислоты по первой ступени диссоциировало 0,05 моль, по второй - 0,0002 моль и по третьей – 0,00000001 моль. Итого образовалось чуть больше 0,1 моль ионов.
Очевидно, этот раствор этой кислоты проводит ток хуже, чем раствор соли.
Пара вопросов для тренировки:
1) Какие частицы образутся при диссоциации нитрата натрия
а) Na + , N +5 , O -2 ; б) Na + , NO 3 - в) Na, NO 2 , O 2 г) NaNO 2 , O 2
Решение: нитрат натрия образован остатком азотной кислоты и катионом натрия. Уравнение его диссоциации: NaNO3 ⇄ Na + + NO 3 - . Ответ б).
2) В четырех пробирках находятся одномолярные растворы следующих веществ:
а) H 3 PO 4 б) Na 2 SO 4 в) NaCl г) HBr
В какой пробирке больше всего ионов?
Решение: a) ортофосфорная кислота – средней силы, диссоциирует слабо, большая часть молекул останутся в растворе молекулами.
б) сульфат натрия – соль, диссоциирует полностью, из одного моль соли олучается три моль ионов: Na 2 SO 4 ⇄ 2Na + + SO 4 2- .
в) хлорид натрия – соль, диссоциирует полностью, из одного моль соли образуется два моль ионов: NaCl ⇄ Na + + Cl - .
г) бромоводородная кислота – сильная, но диссоциирует не полностью (в отличие от солей). В реакции HBr ⇄ H+ + Br- из одного моль HBr образуется меньше двух моль ионов.
Константа гидролиза равна отношению произведения концентраций
продуктов гидролиза к концентрации негидролизованной соли.
Пример 1. Вычислить степень гидролиза NH 4 Cl.
Решение: Из таблицы находим Кд(NH 4 ОН)=1,8∙10 -3 , отсюда
Кγ=Кв/Кд к = =10 -14 /1,8∙10 -3 = 5,56∙10 -10 .
Пример 2. Вычислить степень гидролиза ZnCl 2 по 1 ступени в 0,5 М растворе.
Решение: Ионное уравнение гидролиза Zn 2 + H 2 O ZnOH + + H +
Kд ZnOH +1=1,5∙10 -9 ; hγ=√(Кв/ [Кд осн ∙Cм]) = 10 -14 /1,5∙10 -9 ∙0,5=0,36∙10 -2 (0,36%).
Пример 3. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: a) KCN; б) Na 2 CO 3 ; в) ZnSO 4 . Определите реакцию среды растворов этих солей.
Решение: а) Цианид калия KCN - соль слабой одноосновной кислоты (см. табл. I приложения) HCN и сильного основания КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К + и анионы CN - . Катионы К + не могут связывать ионы ОН - воды, так как КОН - сильный электролит. Анионы же CN - связывают ионы Н + воды, образуя молекулы слабого элекролита HCN. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
CN - + Н 2 О HCN + ОН -
или в молекулярной форме
KCN + Н 2 О HCN + КОН
В результате гидролиза в растворе появляется некоторый избыток ионов ОН - , поэтому раствор KCN имеет щелочную реакцию (рН > 7).
б) Карбонат натрия Na 2 CO 3 - соль слабой многоосновной кислоты и сильного основания. В этом случае анионы соли СО 3 2- , связывая водородные ионы воды, образуют анионы кислой соли НСО - 3 , а не молекулы Н 2 СО 3 , так как ионы НСО - 3 диссоциируют гораздо труднее, чем молекулы Н 2 СО 3 . В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
CO 2- 3 +H 2 O HCO - 3 +ОН -
или в молекулярной форме
Na 2 CO 3 + Н 2 О NaHCO 3 + NaOH
В растворе появляется избыток ионов ОН - , поэтому раствор Na 2 CO 3 имеет щелочную реакцию (рН > 7).
в) Сульфат цинка ZnSO 4 - соль слабого многокислотного основания Zn(OH) 2 и сильной кислоты H 2 SO 4 . В этом случае катионы Zn + связывают гидроксильные ионы воды, образуя катионы основной соли ZnOH + . Образование молекул Zn(OH) 2 не происходит, так как ионы ZnOН + диссоциируют гораздо труднее, чем молекулы Zn(OH) 2 . В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза
Zn 2+ + Н 2 О ZnOН + + Н +
или в молекулярной форме
2ZnSO 4 + 2Н 2 О (ZnOH) 2 SO 4 + H 2 SO 4
В растворе появляется избыток ионов водорода, поэтому раствор ZnSO 4 имеет кислую реакцию (рН < 7).
Пример 4. Какие продукты образуются при смешивании растворов A1(NO 3) 3 и К 2 СО 3 ? Составьте ионно-молекулярное и молекулярное уравнение реакции.
Решение. Соль A1(NO 3) 3 гидролизуется по катиону, а К 2 СО 3 - по аниону:
А1 3+ + Н 2 О А1ОН 2+ + Н +
СО 2- 3 + Н 2 О НСО - з + ОН -
Если растворы этих солей находятся в одном сосуде, то идет взаимное усиление гидролиза каждой из них, ибо ионы Н + и ОН - образуют молекулу слабого электролита Н 2 О. При этом гидролитическое равновесие сдвигается вправо и гидролиз каждой из взятых солей идет до конца с образованием А1(ОН) 3 и СО 2 (Н 2 СО 3). Ионно-молекулярное уравнение:
2А1 3+ + ЗСО 2- 3 + ЗН 2 О = 2А1(ОН) 3 + ЗСО 2
молекулярное уравнение: ЗСО 2 + 6KNO 3
2A1(NO 3) 3 + ЗК 2 СО 3 + ЗН 2 О = 2А1(ОН) 3





